

Editorial: Hospital Metropolitano
ISSN (impreso) 1390-2989 - ISSN (electrónico)2737-6303
Edición: Vol. 29 (suppl 1) 2021 - agosto
DOI: https://doi.org/10.47464/MetroCiencia/vol29/supple1/2021/20-31
URL: https://revistametrociencia.com.ec/index.php/revista/article/view/220
Pág: 20-31
Introducción
El soporte vital avanzado (SVA) incluye un conjunto de técnicas y maniobras cuyo objetivo es restaurar definitivamente la circulación y la respiración espontáneas, minimizando la lesión cerebral anóxica en el paciente que ha sufrido un paro cardiorrespiratorio (PCR). Los resultados mejoran significativamente cuando el soporte vital básico (SVB) se inicia precozmente por las personas que presencian el episodio y el SVA antes de ocho minutos.
Objetivos
Consideraciones generales
Las guías de SVA deben incluir la mejor evidencia científica disponible, y permitir su flexibilización o adaptación a escenarios con infraestructuras médicas de emergencias locales o nacionales dispares, sin que ello signifique un perjuicio en la atención médica. Estas recomendaciones se basan en las premisas que la incidencia de patologías graves en pacientes pediátricos es mucho menor que en los adultos, las respuestas fisiopatológicas son diferentes en estas poblaciones, y que muchas de las emergencias pediátricas son manejadas por personal que no es especialista en pediatría y que tiene experiencia médica de emergencias pediátrica limitada1,2.

El Paro Cardiorrespiratorio (PCR) es el cese brusco, inesperado y potencialmente reversible de la actividad mecánica del corazón y de la ventilación espontánea3. En pediatría es causado en la mayoría de los casos, por hipoxemia y acidosis que son el resultado de la progresión de insuficiencia respiratoria o shock4.
Diagnóstico
Los signos de Paro Cardíaco incluyen:

Ausencia de respuesta al dolor (coma)
Apnea o respiración ineficaz (respiración agónica)

Ausencia de signos de circulación (signos importante vitales)
Palidez o cianosis
La palpación del pulso central (braquial o femoral en el lactante y carotídeo o femoral en el niño) no es un método fiable para decidir la necesidad de inicio de compresiones torácicas, por lo que si el niño no tiene signos vitales deben iniciarse las compresiones torácicas, con la excepción que se esté seguro de poder palpar un pulso arterial central en un lapso de 10 segundos5. La ecografía puede ayudar a detectar actividad cardíaca y algunas causas de paro cardíaco potencialmente reversibles, pero su uso no debe interferir con las maniobras de RCP5-7.
Prevención
Dada la alta tasa de mortalidad del paro cardiorrespiratorio pediátrico, que aumenta aún más cuando no se realizan las maniobras de RCP en forma inmediata, la prevención debe estar focalizada en programas de detección precoz de las enfermedades que predisponen al PCR, (enfermedades respiratorias y sepsis) y también en realizar programas de entrenamiento de RCP en forma periódica para los profesionales de la salud e incluir a la comunidad.
Consideraciones Generales
Secuencia de RCP avanzado:
Asegurar la vía aérea y dar soporte ventilatorio con concentraciones altas de oxígeno (100%).
Monitorizar el ritmo cardíaco, lo que permite orientar y valorar la reanimación.
Obtener un acceso vascular y administrar fármacos y fluidos.
Esta secuencia debe realizarse en forma simultánea, teniendo en cuenta la importancia de no interrumpir el SVB.
Reanimación Cardiopulmonar Básica durante la RCP avanzada:
La utilización de la secuencia C-A-B (Circulación - Apertura de la vía aérea -Ventilación) o A-B-C (Apertura de la vía aérea - Ventilación - Circulación) es indistinta, en ambas se hace énfasis a la realización de RCP de alta calidad, apertura de la vía aérea y ventilaciones efectivas.
Lo esencial en la población pediátrica es asegurar la vía aérea y el inicio en forma temprana y eficaz de la ventilación y oxigenación, dada la alta prevalencia de PC de origen respiratorio.
Se recomienda que cada país enseñe una secuencia única para toda la población.
Manejo de la vía aérea durante el PCR:
La insuficiencia respiratoria es la principal causa de PCR en niños en Latinoamérica, por lo tanto, es muy importante proporcionar una adecuada ventilación y oxigenación durante la RCP tanto básica como avanzada.
Con respecto a la ventilación se debe administrar un volumen corriente apropiado lo que se lograría mediante un aumento normal del diámetro de la pared torácica. La hiperventilación provoca aumento de la presión intratorácica, con disminución de la perfusión cerebral y coronaria, por lo que debe evitarse.

Ventilación coordinada con las compresiones o no coordinada, durante la Ventilación a Presión Positiva (VPP):
Durante la RCP las guías recomiendan usar una relación de 15 compresiones y 2 ventilaciones si el niño no tiene un dispositivo avanzado de la vía aérea.
En el niño intubado, AHA recomienda compresiones continuas y realizar una ventilación cada 2 a 3 segundos (20 a 30 ventilaciones por minuto), ya que nuevos trabajos muestran que frecuencias de ventilación más altas se asocian a mejores índices de retorno a la circulación espontánea y de supervivencia en niños con PCR intrahospitalarios (PCIH)8.
Nuevos datos muestran que frecuencias respiratorias de 30 por minuto en lactantes (menores de un año) y 25 por minuto en niños más grandes se asocian a mejores índices de retorno a la circulación espontánea (RCE) y de supervivencia en situaciones de PCIH. Si bien hay datos insuficientes para identificar el volumen corriente ideal administrado, se recomienda evitar la hiperventilación como se mencionó previamente9.

Una revisión sistemática evaluó la efectividad de los diferentes métodos de compresión-ventilación para la RCP, se observó que los pacientes pediátricos que recibieron RCP con una relación compresión-ventilación de 15: 2 o 30: 2 experimentaron una función neurológica, supervivencia y RCE favorables en comparación con la RCP sólo con manos para niños de todas las edades, pero para niños menores de 1 año, no se observaron diferencias estadísticamente significativas10.
La capnografía puede proporcionar información sobre la efectividad de las compresiones torácicas, pero no se han establecido valores específicos en niños11. También puede utilizarse tanto para la comprobación de la colocación como la monitorización de la colocación del tubo endotraqueal (TET)9.Una EtCO2 baja o ausente puede reflejar un flujo sanguíneo pulmonar bajo o ausente, mientras que un EtCO2 mayor a 15 mm Hg puede ser indicador de reanimación adecuada.La recomendación sigue siendo que en pacientes no intubados, se debe coordinar la VPP con las compresiones y en los pacientes intubados se realizan compresiones continuas sin hacer pausas para las ventilaciones.
Intubación endotraqueal (IOT):
Es razonable el uso de TET con balón tanto para lactantes como para niños. Se debe poner especial cuidado a la presión de insuflación del balón, que se recomienda entre 20 a 25 cm de H2O. Varios estudios y revisiones sistemáticas respaldan su seguridad y demuestran menor necesidad de cambios de tubo y reintubación, así mismo se reduce el riesgo de aspiración, y la estenosis subglótica secundaria al daño laríngeo es poco frecuente si se maneja cuidadosamente la presión de inflado del balón5,9.
La IOT permite asegurar la vía aérea y realizar ventilaciones y compresiones ininterrumpidas, sin embargo no es un procedimiento sencillo, por lo tanto debe ser llevado a cabo por personal entrenado y disponer de los materiales adecuados. No se consideran superiores la intubación endotraqueal o los dispositivos supraglóticos a la ventilación con bolsa y máscara pero la certeza general de la evidencia es de baja a muy baja, se necesitan ensayos de eficacia aleatorios bien diseñados para abordar esta cuestión12. Por lo tanto no se recomiendan ni rechazan el uso de dispositivos avanzados para la vía aérea, dado que con la experiencia y entrenamiento adecuados, el uso de ventilación con bolsa y máscara es una alternativa razonable al uso de un dispositivo avanzado para la vía aérea (IOT o dispositivos supraglóticos) ya que éstos suelen requerir entrenamiento y equipamiento más específicos13.
Sin embargo, si la ventilación con bolsa y máscara es ineficaz a pesar de la optimización apropiada, se debe considerar una intervención con dispositivos avanzados para la vía aérea5,14,15.
No se recomienda el uso rutinario de presión cricoidea durante la IOT ya que nuevos estudios demostraron que reduce el éxito de la intubación y no reduce el riesgo de regurgitación.
Circulación:
El soporte circulatorio incluye:
Compresiones torácicas:
No se ha identificado suficiente evidencia nueva que justificara la realización de nuevas revisiones sistemáticas o la reconsideración de las pautas de reanimación actuales. Existen lagunas significativas en la evidencia de la investigación relacionada con los componentes de la compresión torácica, como ser: la falta de evidencia de alto nivel, la escasez de estudios de PCIH y la falta de consideración de la posibilidad de interacciones entre los componentes de la compresión torácica16.
Los reanimadores deben realizar compresiones torácicas que hundan el tórax del niño al menos 1/3 del diámetro anteroposterior del tórax, lo que equivale a 4 cm en lactantes y 5 cm en niños, tanto en adultos como adolescentes se recomienda una profundidad de compresión de al menos 5 cm y máximo de 6 cm y permitiendo la completa descompresión de la pared torácica luego de cada compresión.Se deben realizar entre 100 a 120 compresiones por minuto con una relación 15:2 de masaje cardíaco y ventilación17,18.
Accesos vasculares:
Son esenciales para la administración de medicamentos y la obtención de muestras de sangre.Se realizó una revisión sistemática sobre el uso de fármacos intravenosos versus intraóseos durante el paro cardíaco. Se identificó un número limitado de estudios, los resultados agrupados de cuatro estudios observacionales favorecieron el acceso intravenoso con pruebas de certeza muy baja. A partir de los análisis de subgrupos de dos ensayos clínicos aleatorios, no hubo interacción estadísticamente significativa entre la vía de acceso y el fármaco de estudio sobre los resultados19.
Dada la necesidad urgente de conseguir un acceso vascular, es muy importante establecer un orden de prioridades basado en los siguientes criterios:
Acceso Intraóseo (IO):
Debe considerarse la vía de elección en el niño en PCR dado que se trata de un acceso rápido y fácil de insertar, logrando una distribución rápida hacia la circulación central. El acceso IO debe mantenerse hasta hallar un acceso intravenoso definitivo. Todos los centros deberían disponer de agujas intraóseas, también es fundamental la formación de los profesionales de la salud en su uso.
Fluidos:
Ritmos de paro:
Se debe monitorizar a todos los pacientes con paro cardiaco, por lo tanto, se debe colocar el monitoreo de ECG tan pronto como sea posible.
Los ritmos asociados a paro cardiaco son los siguientes:
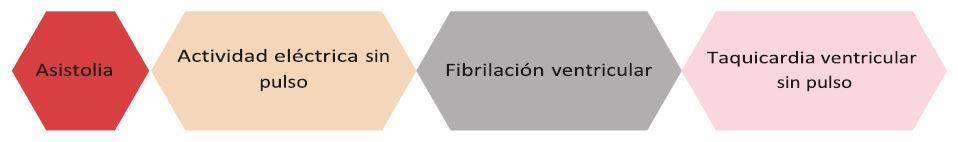
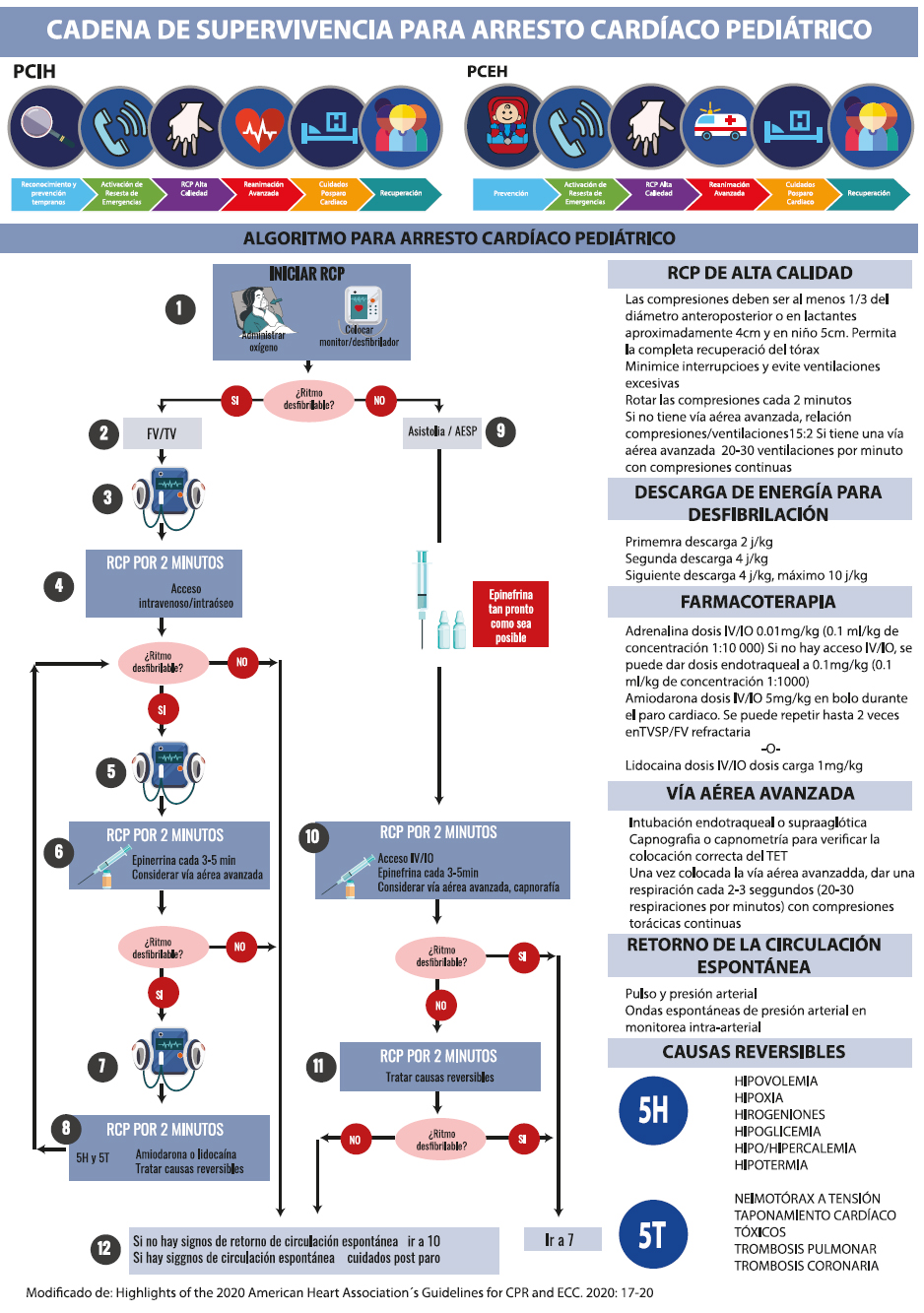
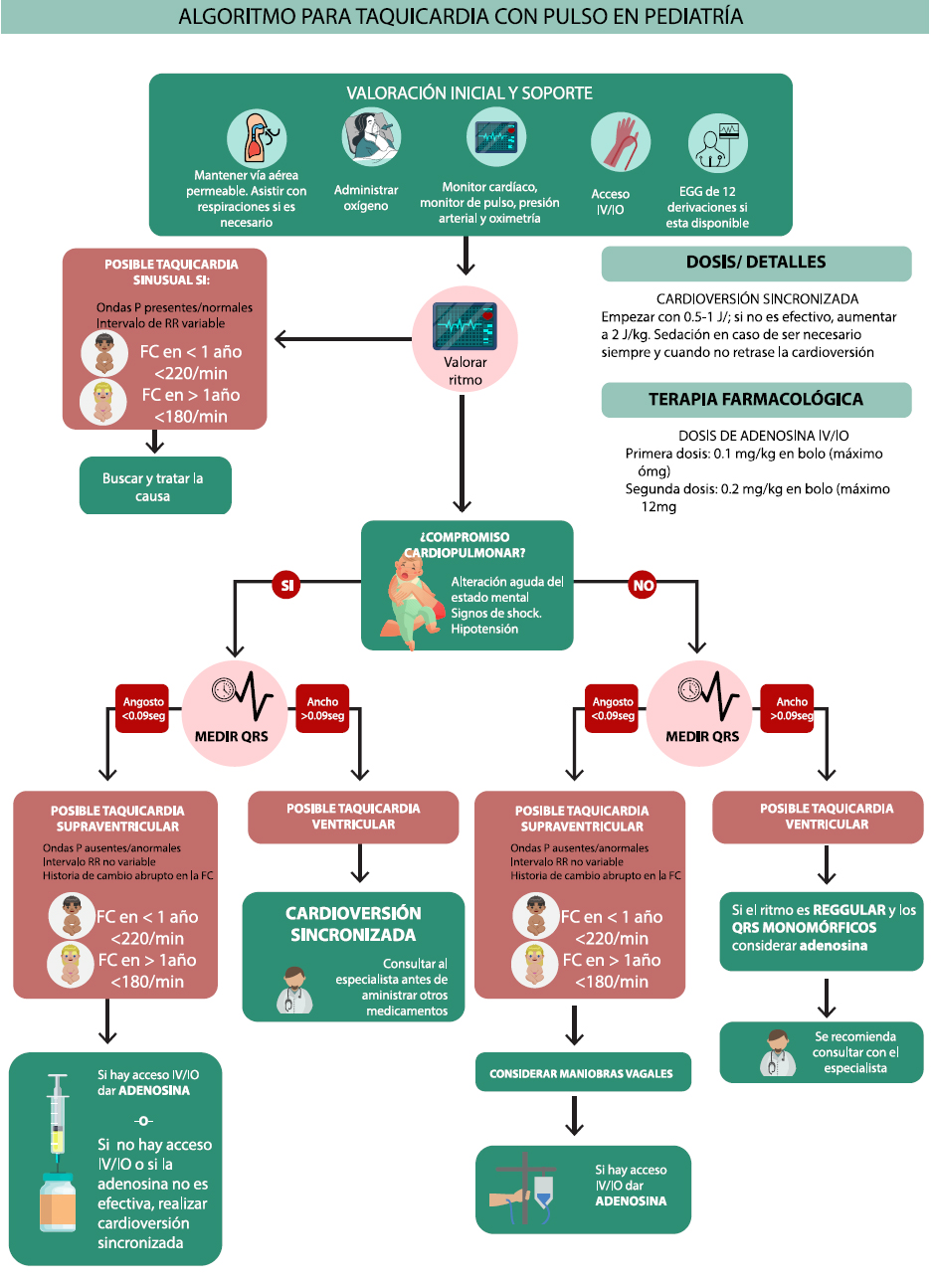
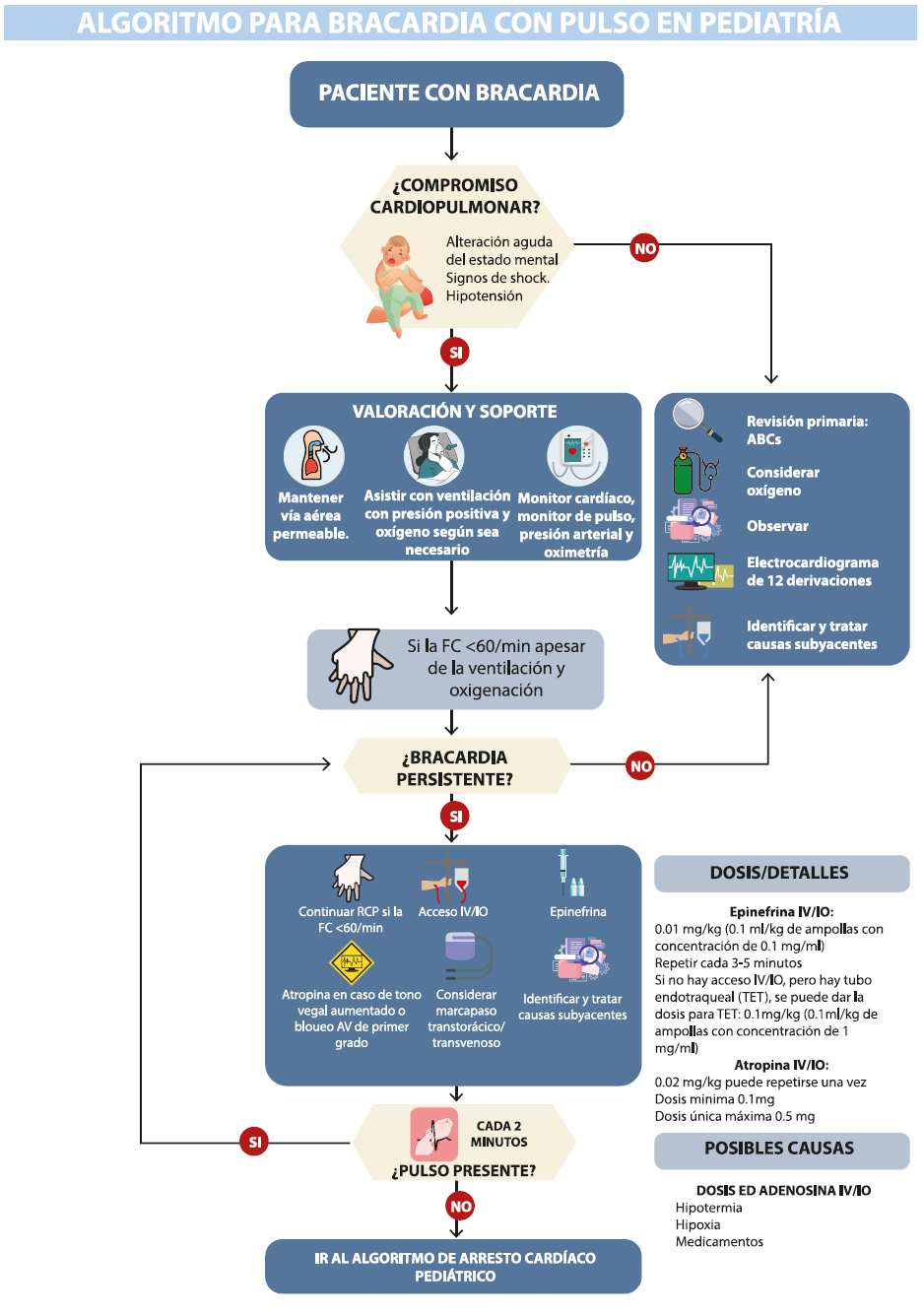
En el paciente pediátrico los ritmos más frecuentemente encontrados en el paro cardiaco son la asistolia y la actividad eléctrica sin pulso. En el anexo se encuentran los algoritmos de manejo del paciente con PCR.
El mismo se divide en dos partes fundamentales de acuerdo al ritmo que presente el paciente:
El diagnóstico y tratamiento de las arritmias no ha sufrido modificaciones en las recomendaciones, para la FV o TVSP refractarias al tratamiento eléctrico se pueden utilizar en forma indistinta amiodarona o lidocaína.
Es razonable la administración de adrenalina durante el paro cardíaco ya que los vasopresores pueden ayudar a restaurar la circulación espontánea al aumentar la presión de perfusión coronaria y ayudar a mantener la perfusión cerebral. La misma debe ser administrada rápidamente en la RCP de ritmos no desfibrilables (recomendación basada en muy baja evidencia)9.
La evidencia disponible no respalda el uso rutinario de atropina antes de la intubación en lactantes y niños críticamente enfermos. Puede ser razonable la utilización de atropina como premedicación en intubaciones de emergencia específicas cuando existe un mayor riesgo de bradicardia.
En todo niño que presente una arritmia se debe comprobar la presencia de signos vitales y pulso central, si no hay signos vitales se debe iniciar RCP, si tiene signos vitales y pulso central debe evaluarse el estado hemodinámico.
Tratamiento eléctrico y farmacológico de las arritmias en los niños
Desfibrilación: La descarga eléctrica inmediata es el tratamiento de elección en la fibrilación ventricular y en la taquicardia ventricular sin pulso.

La dosis de descarga recomendada actualmente continúa siendo de 2 J/kg para la primera descarga, 4 J/kg para la segunda descarga y en las siguientes mayor o igual a 4 J/Kg con una dosis máxima de 10 J/kg o la dosis de adulto21. En Europa se recomienda 4 J/kg para la dosis inicial y las posteriores.
Se deben seleccionar las palas y parches más grandes posibles para lograr un buen contacto con la pared del tórax, debe existir una buena separación entre las palas.
Las medidas recomendadas son 4,5 cm de diámetro para los lactantes y niños con peso menor de 10 Kg y de 8 a 10 cm de diámetro para los que pesan más de 10 Kg. La utilización de parches autoadhesivos facilitan la realización de RCP de alta calidad al disminuir el tiempo de interrupción de las compresiones torácicas para administrar la descarga eléctrica5.
Un tamaño apropiado de paleta o almohadilla autoadhesiva es:
Tamaño "adulto" (8 a 10 cm) para niños de más de 10 kg (aproximadamente > 1 año) Talla "infantil" para bebés menores a 10 kg (AHA)
Las palas deben aplicarse firmemente sobre el tórax en posición anterolateral, una debajo de la clavícula derecha y la otra en la axila izquierda5,21. Si no se dispone de palas pediátricas, se pueden utilizar en los lactantes las palas de adulto suficientemente separadas o una en la parte anterior del tórax a la izquierda del esternón y otra en la espalda debajo de la escápula izquierda9.
Monitorización durante la RCP avanzada:
Drogas utilizadas durante la RCP:
Adrenalina: es la droga utilizada en todos los ritmos de PCR, por su efecto alfa adrenérgico aumenta la presión arterial y con ello aumenta el flujo coronario.
Se enfatiza la administración temprana, es razonable su uso dentro de los 5 minutos de iniciadas las compresiones torácicas9.
En pacientes con PCIH con ritmo no desfibrilable, un estudio demostró que por cada minuto de demora en la administración de adrenalina, hubo una disminución significativa del RCE, la supervivencia a las 24 hs, la supervivencia al alta y la supervivencia con resultado neurológico favorable.
Los pacientes que recibieron adrenalina en un plazo de 5 minutos después del inicio de la RCP comparados con los que recibieron adrenalina en un plazo mayor, fueron más propensos a sobrevivir a las descargas.
Dosis 0,01 mg /kg (0,1 ml/kg de la concentración 0,1 mg/ml) cada 3 a 5 minutos. Si no hay acceso vascular y el TET está en posición, administrar 0,1 mg/kg (0,1 ml/kg de la concentración 1 mg/ml)23,28.
Amiodarona: antiarrítmico que se utiliza en la FV y TV sin pulso posterior a la tercera descarga y primera dosis de adrenalina. Se puede administrar IV o IO. Su dosis es 5 mg/kg y puede repetirse 2 veces más.
Lidocaína: antiarrítmico utilizado para el tratamiento de la FV o TV sin pulso que no responde al tratamiento eléctrico (3 descargas) y a la primera dosis de adrenalina.
Su dosis es 1 mg/kg, con buena respuesta continuar con infusión continua 20-50 mcg/kg/min. Se considera de primera línea junto con la amiodarona. (29)
Atropina: 0,02 mg/kg. Se puede repetir una vez. Dosis mínima 0,1 mg y dosis única máxima de 0,5 mg9. La evidencia disponible no respalda el uso rutinario de atropina antes de la intubación en lactantes y niños críticamente enfermos. Puede ser razonable que se utilice atropina como premedicación en intubaciones de emergencia específicas cuando existe un mayor riesgo de bradicardia.
Sulfato de magnesio: indicada en el PCR en las arritmias graves asociadas a hipomagnesemias y en las torsades de pointes. Su dosis es de 25 – 50 mg/kg, máximo 1 gramo.
Gluconato de calcio: indicado sólo en el paro cardíaco asociado a hipocalcemia comprobada, en la intoxicación con bloqueantes de los canales de calcio, hipermagnesemia e hiperkalemia.Su dosis es 50 mg/kg. Máximo 1 gramo.
Glucosa: indicada en caso de hipoglucemia severa confirmada.Su dosis es 2 ml/kg Dx 25 % o 5 ml/kg Dx 10 %
Bicarbonato de sodio: sólo indicado en el paro cardíaco prolongado, en situaciones de acidosis metabólica severa y en intoxicación con antidepresivos tricíclicos.Su dosis es 1 – 2 meq/kg.

Para la prevención del PCR es fundamental la capacitación en RCP de los profesionales de la salud y de la comunidad. Se deben desarrollar protocolos de manejo del PCR, creando equipos de resucitación o equipos de respuesta rápida conformados por médicos y enfermeros, con dinámica de equipo y roles definidos para cada miembro, con la finalidad de detectar e iniciar en forma precoz el tratamiento de las emergencias. Posterior a cada paro cardiaco se recomienda que los miembros del equipo realicen un debriefing.
Conceptos básicos:
La causa más frecuente de PCR en pediatría es la hipoxia.
Es fundamental la prevención y la atención temprana de las patologías que llevan al PCR.
El diagnóstico del PCR es clínico, al encontrar ausencia de respuesta, cese en la respiración (o respiraciones inefectivas) y ausencia de pulso palpable.
La premisa en la RCP es seguir los protocolos para garantizar RCP de alta calidad.
El entrenamiento y la organización del equipo de salud según la disponibilidad de recursos locales es importante en la atención de los pacientes en PCR.
Recomendaciones
Cada país debe diseñar su propio algoritmo basado en las recomendaciones internacionales según su disponibilidad de recursos, asegurando la administración de RCP de alta calidad en todo momento.
Se debe poner énfasis en la prevención y atención precoz de las patologías que llevan al deterioro hemodinámico de la población pediátrica.
Con respecto a la vía aérea y ventilaciones se debe tener presente la premisa de evitar la hiperventilación y mantener la frecuencia recomendada para la edad.
La recomendación sigue siendo que en pacientes no intubados, se debe coordinar la VPP con las compresiones y en los pacientes con vía aérea avanzada se realizan compresiones continuas sin hacer pausas para las ventilaciones.
Se recomienda que cada país enseñe una secuencia única para toda la población.
Los dispositivos utilizados pueden ser bolsa y máscara o tubo endotraqueal, por lo que es recomendable el entrenamiento en una técnica para instrumentar el manejo de la vía aérea según la disponibilidad local del material. Se pueden utilizar tubos endotraqueales sin o con balón en la emergencia, sin embargo se prefieren los tubos con balón para reducir la fuga de aire y reducir la necesidad del recambio de tubos.- Monitorear la calidad de la RCP mediante presión arterial invasiva, CO2 espirada, ecografía y NIRS. Estos últimos requieren estudios para estandarizar su uso. Sin embargo, la imposibilidad de contar con estos recursos no limita la capacidad de administrar RCP de alta calidad.
La administración de drogas durante RCP enfatiza la necesidad de la colocación de un acceso vascular, por ello se requiere material idóneo y entrenamiento para la colocación de un acceso venoso endovenoso durante la emergencia, o intraóseo ante la imposibilidad de colocación del previo.
La documentación de los procedimientos realizados y sus resultados proporcionan información valiosa que permitirán en un futuro actualizar las normas con las que se rige la reanimación a nivel mundial.
Conclusión
En el transcurso de los últimos años se ha incrementado en manera importante la sobrevida de los pacientes que han sufrido un paro cardiorrespiratorio intrahospitalario. Actualmente se reporta un retorno a la circulación espontánea en 64% a 77% de los pacientes y una sobrevida al alta hospitalaria de 43%, sin incrementarse el porcentaje de discapacidad neurológica. Esto se ha logrado gracias a la reanimación cardiopulmonar de alta calidad y a los avances en los cuidados posteriores en terapia intensiva20,30-32. Es de vital importancia el entrenamiento y actualización continuos, al alcance de todos los participantes en la atención de pacientes pediátricos críticos, y el desarrollo de protocolos locales y adaptados a las disponibilidades y necesidades de cada lugar de América Latina. Esto sólo se logra con el apoyo y el trabajo en conjunto de todos los países que la conforman.
REFERENCIAS BIBLIOGRÁFICAS
Dra. Mariana Cyunel M.D.
Especialista en Terapia Intensiva Pediátrica.UCIP.
Hospital de Niños Ricardo Gutiérrez.
Ciudad Autónoma de Buenos Aires. Argentina
https://orcid.org/0000-0002-4432-2162
Dra. Marcela Cuartas. M.D.
Hospital de Alta Complejidad en Red "El Cruce" Buenos Aires, Argentina
https://orcid.org/0000-0002-4099-7963
Dra. Norma Raúl M.D.
Pediatra Intensivista
Hospital de Alta Complejidad en Red
"El Cruce"Universidad Nacional Arturo Jauretche
Florencio Varela, Buenos Aires, Argentina
https://orcid.org/0000-0001-5996-6836
Cyunel M, Cuartas M, Norma R. Soporte vital avanzado pediátrico. Metro Ciencia [Internet]. 30 de agosto de 2021; 29(Supple1):20-31. https://doi.org/10.47464/MetroCiencia/vol29/supple1/2021/20-31