
ARTÍCULOS EN REVISIÓN
Fluidoterapia en pediatría:
solución salina vs. soluciones balanceadas
Fluid Therapy in pediatrics: normal saline vs. balanced solutions

ARTÍCULOS EN REVISIÓN
solución salina vs. soluciones balanceadas
Fluid Therapy in pediatrics: normal saline vs. balanced solutions
Recibido: 28-04-2022
Aceptado: 03-05-2022
Publicado: 30-06-2022
DOI: https://doi.org/10.47464/MetroCiencia/vol30/2/2022/50-65
Revista MetroCiencia
Volumen 30, Número 2, 2022
Editorial Hospital Metropolitano
Alfredo Carlos Rodríguez Portelles1, Santiago Campos Miño2
RESUMEN
Introducción: La elección de la solución cristaloide de resucitación en pediatría es uno de los tópicos más controversiales de la práctica pediátrica moderna. La gran variabilidad de criterios y evidencias por parte de la comunidad médica internacional, producen una duda científica razonable que justifica explorar el estado del arte sobre el uso en niños de solución salina versus soluciones balanceadas para resucitación. Método: Revisión bibliográfica en las bases de datos Pubmed, Scielo, EBSCO, Cochrane Library Plus, Scopus, y Medline Plus. Se seleccionaron 51 artículos publicados, fundamentalmente, en los últimos cinco años, en idioma español o inglés, así tambien como se examinaron las recomendaciones de guías internacionales sobre fluidoterapia de resucitación en pediatría. Resultados: Se describe el trasfondo fisiológico y ácido/básico que justifica las indicaciones y efectos adversos de los cristaloides endovenosos. Se identifican las ventajas y usos clínicos de los mismos. Se discuten las evidencias de su uso en diversas entidades como sepsis y shock séptico, cetoacidosis diabética, diarrea y deshidratación, entre otros. Conclusiones: A diferencia de recientes resultados en estudios de adultos, la evidencia en niños ha demostrado que las soluciones balanceadas disminuyen el riesgo de lesión renal aguda y la necesidad de terapia de reemplazo renal. Existen sólidos resultados que respaldan el uso de soluciones balanceadas en la resucitación de la cetoacidosis diabética pediátrica. Se propone utilizar la fluidoterapia de resucitación con cristaloides en pediatría de manera individualizada, en respuesta al sustrato fisiológico de la entidad clínica de cada paciente.
Palabras clave: fluidoterapia, solución salina, soluciones cristaloides, ringer lactato, pediatría, resucitación
ABSTRACT
Introduction: the choice of the resuscitation crystalloid solution in pediatrics is one of the most controversial issues in modern pediatric practice. There is variable criteria and evidence for their use within the international medical community. Therefore, there is a reasonable scientific doubt to sustain the need of exploring the state of the art on the use of normal saline versus balanced crystalloids for resuscitation in children. Method: An exhaustive bibliographic review was carried out in the Pubmed, Scielo, EBSCO, Cochrane Library Plus, Scopus, and Medline Plus databases. Fifty-one articles published, fundamentally, in the last five years, in Spanish or English, were selected, as well as the recommendations of international guidelines on resuscitation fluid therapy in pediatrics. Results: The physiological and acid/base background that justifies the indications and adverse effects of intravenous crystalloid administration is described. Advantages and clinical uses are identified. Evidence of use in various entities such as sepsis and septic shock, diabetic ketoacidosis, diarrhea, dehydration, and others are discussed. Conclusions: Contrary to recent results in adult studies, evidence in children has shown that balanced solutions decrease the risk of acute kidney injury and the need for renal replacement therapy. There are solid results that support the use of balanced solutions in the resuscitation of pediatric diabetic ketoacidosis. It is proposed that the use of crystalloid resuscitation fluid therapy in pediatrics should be individualized in response to the physiological substrate of the clinical entity of each patient.
Keywords: fluid therapy, normal saline, crystalloids, balanced solutions, Ringer's Lactate, pediatrics, resuscitation.
Alfredo Carlos Rodríguez Portelles
 https://orcid.org/0000-0001-6920-0527
https://orcid.org/0000-0001-6920-0527
Santiago Campos Miño
 https://orcid.org/0000-0003-4686-7358
https://orcid.org/0000-0003-4686-7358
 |
Este artículo está bajo una licencia de Creative Commons de tipo Reconocimiento – No comercial – Sin obras derivadas 4.0 International. |
*Correspondencia: acrodriguezpor@gmail.com
Introducción
Una de las piedras angulares de la atención médica pediátrica moderna es la utilización de la fluidoterapia endovenosa en situaciones de resucitación hídrica. La fluidoterapia intravenosa ha sido fundamental para la atención de la emergencia médica durante más de un siglo. Cada año, más de 30 millones de pacientes reciben líquidos intravenosos para reanimación, mantenimiento del volumen intravascular o para diluir medicamentos1. Las soluciones cristaloides son los líquidos intravenosos que se administran con mayor frecuencia y están compuestas de electrolitos disueltos en agua que pasan fácilmente del espacio vascular al intersticio2.
La elección del cristaloide es, sin embargo, bastante variable y sin una base de evidencia clara. En Estados Unidos y Europa, la solución salina al 0,9 % (SS), conocida también como “solución salina normal” o “suero fisiológico”, es el cristaloide más utilizado, especialmente en la práctica pediátrica3. Sin embargo, en la actualidad muchos cirujanos, anestesiólogos e intensivistas prefieren las llamadas “soluciones balanceadas”, cuya concentración de electrolitos se parece más al plasma y tienen capacidad buffer (amortiguadora), como Ringer Lactato (RL), Sterofundin, o Plasma-Lyte A (PL)4.
La variabilidad de selección del líquido óptimo para la reanimación ha escalado hasta convertirse en uno de los tópicos más controversiales de la práctica médica moderna. En los últimos años se han potenciado las investigaciones sobre los efectos de las soluciones balanceadas y no balanceados en población pediátrica y su asociación con mortalidad y otras variables de interés clínico. Por convención, en la práctica médica cotidiana, la mayoría de los pacientes reciben SS 0,9%, pero las evaluaciones clínicas y preclínicas han cuestionado esta práctica. La reposición de líquidos con SS en población pediátrica se ha asociado con efectos adversos microcirculatorios y macrocirculatorios, como lesión renal aguda (LRA), vasoconstricción renal y acidosis metabólica hiperclorémica5,6. Además, varios ensayos clínicos randomizados en niños sostienen que las soluciones cristaloides balanceadas (p. ej., RL y PL), en comparación con SS, tienen el potencial de ser eficaces con menos efectos adversos. Los resultados investigativos declaran que las diferencias importantes entre los cristaloides balanceados y la SS incluyen el contenido de cloruro (SS 154 mEq/L; balanceadas 95-127 mEq/L) y la capacidad amortiguadora medida de acuerdo a la diferencia de iones fuertes (SS 0 mEq/L; balanceadas 25,5-50 mEq/L). Por otra parte, resultados recientemente publicados de minuciosas revisiones sistemáticas, metanálisis y ensayos clínicos randomizados en adultos, como los ensayos BaSICS, PLUS y el de Hammond et al.7–9, han demostrado muy poca diferencia entre SS y soluciones balanceadas, y su asociación con mortalidad y desarrollo de LRA no respaldan el uso preciso de soluciones balanceadas sobre la SS.
Ante estos resultados, es recomendable realizar más estudios comparativos en niños y no extrapolar en exceso resultados de estudios en adultos a población pediátrica. Guías internacionales recientes como la Surviving Sepsis Campaign, en su edición especial de 2020 para pediatría5, las del National Institute for Health and Care Excellence (NICE)10 y estudios aleatorios randomizados11–14, ofrecen una evidencia interesante y robusta para generar una saludable incertidumbre y, de esta manera, replantearse algunos conceptos e indicaciones sobre la decisión de administrar SS o solución balanceada en la resucitación pediátrica. La presente revisión pretende describir el estado del arte actual del uso de la SS 0,9% y las soluciones balanceada en pacientes pediátricos, abordando desde el trasfondo fisiológico hasta las evidencias particulares de su administración como fluidos de resucitación en sepsis y shock séptico, cetoacidosis diabética, diarrea y deshidratación, entre otros, así como su asociación con mortalidad y desarrollo de LRA.
MÉTODOS
Se realizó una exhaustiva revisión bibliográfica de los artículos publicados en inglés o español en los últimos 5 años en las bases de datos Pubmed, Scielo, EBSCO, Cochrane Library Plus, Scopus, y Medline Plus. Se seleccionaron 51 artículos, y se examinaron las recomendaciones de guías internacionales sobre fluidoterapia de resucitación en pediatría como la Surviving Sepsis Campaign 2020 y las guías NICE. Se analizó la información con el objetivo de identificar los conceptos y evidencia actuales concernientes a la utilización de fluidos balanceados y SS en la resucitación hídrica pediátrica. Se utilizó la siguiente estrategia de búsqueda en las bases de datos antes mencionadas: ("Fluid Therapy"[Mesh]) and "Crystalloid Solutions"[Mesh]) and "Saline Solution"[Mesh]) and "Ringer's Lactate"[Mesh]) and "Plasmalyte A" [Supplementary Concept]) and "Resuscitation"[Mesh]) and "Pediatrics"[Mesh].
Fisiología: el faro de la fluidoterapia
Para comprender el efecto fisiológico causado por la administración endovenosa de cristaloides y el trasfondo que sustenta sus beneficios y efectos adversos, en particular sobre la composición de los fluidos corporales, es necesario comprender la teoría de Stewart sobre el equilibrio ácido/base. Se trata de un enfoque cuantitativo, en el que el bicarbonato es una variable que depende de la concentración de sodio y cloro, los llamado iones fuertes, siendo el principal determinante de su concentración la "diferencia de iones fuertes" (DIF), es decir, el espacio potencial de bicarbonato generado por la diferencia entre la concentración de sodio y cloruro en los fluidos corporales15. Una crítica clave del enfoque tradicional, que está centrado en el bicarbonato, es que se trata simplemente de una descripción matemática del pH y no proporciona ningún conocimiento mecánico sobre el aumento y la disminución de hidrogeniones [H+]. En otras palabras, en términos del pH, no hay nada único en el bicarbonato. En consecuencia, la ecuación de Henderson-Hasselbalch puede llevar a los médicos a un “computo”, falacia “ergo-est” (lo calculo, luego es)16.
En respuesta a estas deficiencias, Peter Stewart propuso un análisis ácido/base cuantitativo a fines de la década de 1970 que, según se argumenta, brinda verdaderas relaciones de causa y efecto entre variables independientes y dependientes, respectivamente17. Se refiere a los principios de neutralidad electrónica, en donde:
Stewart propuso que el equilibrio ácido/base agudo está determinado por el dióxido de carbono, los ácidos débiles y la DIF. Los iones fuertes están casi completamente ionizados en solución, y la diferencia de iones fuertes en plasma se define como18:

DIF efectiva: mide la carga neta de los iones, considerando, además, los otros aniones pesados en el organismo y que se presentan de manera importante en estados patológicos. ¿Es “fisiológica” o “normal” la solución salina 0,9%? A pesar de que se denomina "fisiológica” o “normal", la SS 0.9% no es fisiológicamente normal debido a que, en primer lugar, tiene una concentración de cloruro más alta que el plasma, 154 vs. 100 mEq/L; y, en segundo lugar, tiene una DIF diferente a la del plasma, 0 vs. 40 mEq/L. De acuerdo con el enfoque fisicoquímico de Stewart para describir el equilibrio ácido/base, el pH del líquido está determinado en parte por la DIF, que es la suma de las concentraciones de cationes fuertes en la solución (p. ej., sodio, potasio, magnesio), menos la suma de las concentraciones de aniones fuertes en la solución (p. ej., cloruro y lactato). La DIF del líquido extracelular es de aproximadamente 40 mEq/l, mientras que la DIF de la SS 0,9% es 0,19. Stewart propuso que los cambios en la diferencia de iones fuertes alteran directamente el pH del plasma. Si se administra un gran volumen de SS 0,9% por vía intravenosa, se reducirá la DIF en el plasma a través de un mayor aumento relativo en el cloruro en comparación con el sodio. Esta reducción en la DIF aumentará la disociación del agua en H+ y OH-, lo que conducirá a acidosis metabólica17. Para ilustrar este fenómeno, se observa en la figura 1 el efecto de 50 mL/kg de cristaloides intravenosos sobre la DIF en plasma en un niño de 20 kg, anúrico, después de un trasplante de riñón. Un cambio significativo en la DIF es producido por la SS 0,9%, por lo tanto, provocando acidosis metabólica. El efecto de las soluciones de RL, Ionosteril y Sterofundin en la DIF del plasma es menor y el de PlasmaLyte es insignificante, por lo que no tiene un efecto significativo en el equilibrio ácido/base del paciente.
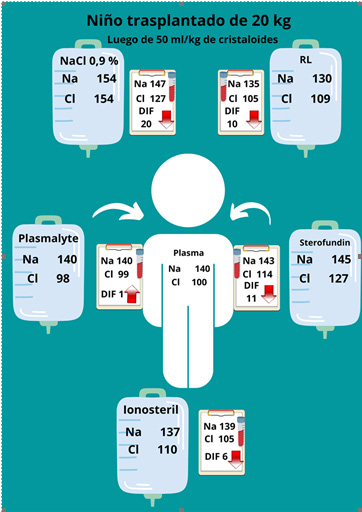
La SS a menudo se considera una solución relativamente hipertónica porque la suma de sus componentes osmóticamente activos (sodio 154 mmol/L + cloro 154 mmol/L) da una osmolalidad teórica in vitro de 308 mOsm/kg H2O. Sin embargo, la SS 0,9% se denomina, en general, solución isotónica, ya que sus componentes son solo parcialmente activos, con un coeficiente osmótico de 0,926. La osmolalidad (tonicidad) calculada in vivo de la SS 0,9% es 285 mOsm/kgH2O, que es la misma que la osmolalidad del plasma19. En el caso de un pH neutro, debido a las condiciones alcalóticas superpuestas, es posible que no se reconozca la acidosis. Esta condición oculta puede revelarse calculando la DIF; si disminuye y tiende a estar por debajo de 40 mEq/L, se desarrolla acidosis. Puede existir acidosis sin hipercloremia. Todas las soluciones salinas (no solo al 0,9%) y las soluciones de dextrosa en agua, tienen una DIF de cero y provocarán acidosis20. Por ejemplo, la SS 0,45% tiene exactamente el mismo efecto que la SS 0,9%. La única diferencia es que cuando se administran ambas el sodio desciende más rápido que el cloro para la SS 0,45%. Sin embargo, el efecto sobre la DIF es el mismo21.
Cristaloides isotónicos balanceados
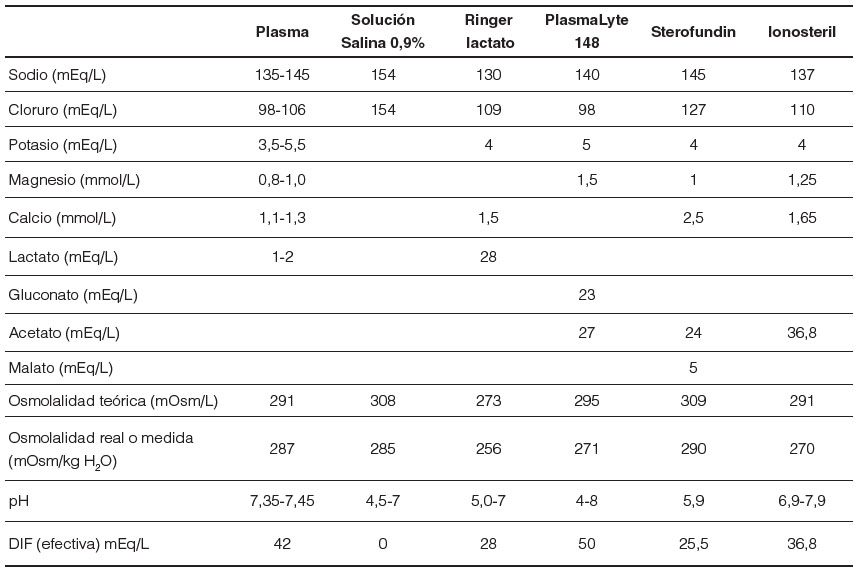
Aunque hay muchos fluidos cristaloides equilibrados disponibles en el mercado, los más utilizados son el lactato de Ringer, el Sterofundin® y el Plasmalyte®, que solo varían en términos del tipo y la cantidad de aniones llamados precursores de bicarbonato. La DIF in vitro del lactato de Ringer es 0 y contiene 28 mEq/L de lactato. Sin embargo, después de la infusión, el lactato desaparece al convertirse en bicarbonato, por lo que in vivo, la DIF aumenta a 28 mEq/L. Stereofundin presenta como amortiguadores al malato 5 mEq/l y 24 mEq/ L de acetato lo que le confiere una DIF efectiva de 25,5 mEq/L. Así mismo, Plasmalyte contiene 50 mEq/L de aniones con 27 mEq/L de acetato y 23 mEq/L de gluconato, los que actúan como amortiguadores, generando una DIF in vivo de 50 mEq/L. En realidad, lactato, gluconato, acetato y malato no se convierten en bicarbonato, sino que entran directamente en el ciclo de Krebs y finalmente se metabolizan. Cuanto mayor sea el valor de DIF in vivo del líquido, más tendencia existe hacia la alcalosis. Por lo tanto, los cristaloides isotónicos balanceados pueden ser una buena opción para neutralizar o prevenir la acidosis relacionada con la administración de fluidos intravenosos22. En la tabla número 2 se observa la composición de las soluciones de cristaloides más usadas, su comparación con el plasma humano, así como su DIF efectiva y osmolalidad. Existen algunas limitaciones para el uso de líquidos balanceados. En primer lugar, en presencia de disfunción hepática, disfunción renal oligúrica, hiperpotasemia y daño cerebral, deben usarse con precaución. En segundo lugar, el hecho de que estos fluidos no puedan utilizarse para la dilución de fármacos también es una limitación. Sin embargo, vale la pena mencionar que en dos ensayos aleatorizados que compararon lactato de Ringer y SS normal durante el trasplante renal, se observó menos hiperpotasemia en el primer grupo22,23.
Una pregunta común es si los líquidos balanceados que contienen potasio (RL y PlasmaLyte) son seguros para usar en pacientes con hiperpotasemia. ¡La respuesta es SÍ! A pesar de contener potasio, estos fluidos aún disminuirán el nivel de potasio sérico de un paciente con hiperpotasemia. Esto se debe a que la concentración de potasio en estos fluidos es más baja en relación con el nivel de potasio sérico del paciente y mucho más baja que la concentración de potasio intracelular del paciente.
Un análisis secundario del ensayo SMART24 no encontró una diferencia en la hiperpotasemia severa (K ≥7 mEq/L) en pacientes hiperpotasémicos que recibieron un líquido balanceado (8,5%) frente a los que recibieron solución salina normal (14%) (p=0,24)
El mito de que debe evitarse RL en la hiperpotasemia no solo es incorrecto, sino probablemente al revés. Para un paciente hiperpotasémico con insuficiencia renal, se debe preferir la RL a la NS. Se ha demostrado que RL produce niveles más bajos de potasio in vivo. Comprender el efecto que tendrá un cristaloide en las concentraciones séricas de potasio implica considerar los efectos sobre la fisiología ácido-base y los cambios de potasio intracelular, que son más importantes que la cantidad de potasio en la bolsa de plástico25.
En los cristaloides isotónicos balanceados se puede encontrar una pequeña cantidad de potasio, como 4-5 mEq/L; esto no se considera tan riesgoso como la hiperpotasemia inducida por acidosis. En caso de insuficiencia hepática, RL puede causar acidosis láctica, ya que se reduce el aclaramiento de lactato20.
Para un paciente con hiperpotasemia y acidosis metabólica, el bicarbonato isotónico probablemente sea superior a RL, ya que puede causar una mayor disminución del potasio sérico. Asimismo, para un paciente con acidosis metabólica, Plasmalyte o Normosol podrían ser preferibles a RL porque estos cristaloides equilibrados son más alcalinizantes. Sin embargo, RL no está contraindicado y ciertamente sigue siendo preferible a SS25.
Se agrega además que las soluciones balanceadas se encuentran de manera general menos disponibles y son más costosas26, por ejemplo, en Ecuador, RL es más caro que SS (media de $1,70 por 1 L de RL frente a media de $1,45 por 1 L de SS al 0,9%).
Hacia dónde apunta la evidencia en pediatría.
A continuación, presentamos los sustentos que existen en la literatura para el uso de los cristaloides isotónicos balanceados en diversos escenarios clínicos.
Diarrea y deshidratación
Desde el año 2005 la Organización Mundial de la Salud (OMS) recomienda RL como primera opción y SS 0,9% como segunda opción para la rehidratación intravenosa rápida en la diarrea infantil y la deshidratación grave27. Las guías NICE, en su actualización del 2020, sugieren utilizar cristaloides isotónicos que contengan sodio en el rango de 131 a 154 mEq/L10. Las guías de la Sociedad Europea de Gastroenterología, Hepatología y Nutrición Pediátrica (ESPGHAN)/Sociedad Europea de Enfermedades Infecciosas Pediátricas (ESPID) aconsejan el uso de SS 0.9% y RL solo en shock grave28. Por otra parte, la Asociación Americana de Pediatría (AAP), desde 1996, advoca el uso de ambas soluciones para la deshidratación causada por diarrea grave29.
En estudios pediátricos como el de Mahajan et al30, los niños con diarrea aguda y deshidratación grave recibieron RL o SS 0,9%, 100 ml/kg durante tres o seis horas. Los 22 pacientes fueron reevaluados después de tres o seis horas. No hubo diferencias en la mejoría del pH, de 7,17 (0,11) a 7,28 (0,09) con RL, en comparación con 7,09 (0,11) a 7,21 (0,09) con SS 0.9%, p = 0,1730. Kartha et al.13 compararon la efectividad del RL versus SS 0,9% en 68 niños de 1 mes a 12 años con deshidratación diarreica aguda severa (clasificación de la OMS); se les administró 100 ml/kg del líquido intravenoso asignado según el plan C de la OMS. Concluyeron que, en la deshidratación diarreica severa aguda, la reanimación con RL y SS 0.9% se asoció con una mejoría clínica y resolución bioquímica similar. Por lo tanto, recomendaron la SS 0.9% debido a la relación costo, disponibilidad e igualdad de mejoría clínica13.
Naseem et al.14, en un ensayo controlado aleatorizado de equivalencia, analizaron ambas soluciones y su asociación con el cambio del sodio sérico durante la corrección de la deshidratación severa en niños con diarrea aguda según el plan C de la OMS. Incluyeron 72 niños de 1 a 12 años con diarrea aguda en los cuales la diferencia en los niveles medios de sodio sérico, en comparación con el valor inicial, fueron en los grupos RL y SS 0.9% fue de 1,4 (4,5) mEq/L y 2,1 (4,9) mEq/L, respectivamente (p=0,58). De esta manera, concluyeron que, tanto RL como SS 0.9%, son equivalentes en términos de cambio en el sodio sérico cuando se usan para la rehidratación intravenosa en niños con diarrea aguda y deshidratación severa14.
Cetoacidosis diabética
La cetoacidosis diabética (CAD) se caracteriza por una fisiología única que incluye acidosis metabólica de leve a grave, y un déficit importante de líquidos. Por lo tanto, los efectos comparativos de los cristaloides balanceados y la SS 0,9% en pacientes con CAD no pueden extrapolarse de otras poblaciones31. La evidencia de estudios observacionales sugiere que la hipercloremia en pacientes con CAD se asocia con un tiempo más largo para la resolución de la misma y una estancia hospitalaria más prolongada32,33.
En un análisis de subgrupos de adultos con CAD de 2 ensayos complementarios, SS 0,9% versus RL o PlasmaLyte en el departamento de emergencias (SALT-ED); y, el ensayo de soluciones isotónicas y eventos renales adversos mayores (SMART), se demostró que, en comparación con la SS 0,9%, el tratamiento con cristaloides balanceados resultó en una resolución más rápida de la CAD, lo que sugiere que los cristaloides balanceados pueden preferirse a la SS 0,9% para el tratamiento agudo de adultos con CAD34. Una revisión retrospectiva de 49.737 pacientes pediátricos con CAD, encontró que el uso de RL se asoció con un menor costo total y un menor riesgo de edema cerebral35. Alghamdi et al31, en un metanálisis con 482 pacientes pediátricos con CAD, concluyeron que el uso de SS 0,9% puede estar asociado con un tiempo más prolongado para la resolución de la CAD, niveles más altos de cloruro sérico posteriores a la reanimación, niveles más bajos de bicarbonato sérico posteriores a la reanimación y una estancia hospitalaria más prolongada en comparación con los cristaloides balanceados.
A la espera de más investigaciones, estos datos, aunque de certeza baja a moderada, respaldan el uso de cristaloides balanceados en lugar de SS 0,9% en la reanimación con líquidos en pacientes pediátricos con CAD.
Neurocríticos y neuroquirúrgicos
A pesar de las preocupaciones de seguridad con respecto a la hipercloremia, el uso de SS 0,9% sigue siendo el estándar de atención en pacientes neuroquirúrgicos y con lesión cerebral, ya que su contenido suprafisiológico de sodio puede proteger contra el edema cerebral. Sin embargo, en estudios como el de Roquilly et al.36, donde se incluyeron 42 pacientes con traumatismo craneoencefálico severo, se observó una mayor incidencia de acidosis hiperclorémica con SS 0,9% en comparación con las nuevas soluciones balanceadas, sin una diferencia en presión intracraneal, diferencia de medias 4 mmHg [-1, 8]; p= 0,088)36.
En estudios pediátricos, como el de Lima et al37, donde se analizaron los electrolitos séricos antes, durante y en el primer día del postoperatorio de resección tumoral de 53 pacientes (rango de edad 6 meses a 12 años), se concluyó que la infusión de SS 0,9% resultó en una mayor variación del cloruro sérico al comparar el valor de antes con el de después de la cirugía. La infusión de cristaloides balanceados se asoció con un perfil electrolítico y ácido/base más seguro en comparación con el uso de SS 0,9%37.
Cirugía general de alta complejidad
En el estudio de Disma et al.38 se incluyeron un total de 240 pacientes programados para cirugía mayor con edades entre 1 y 36 meses en los dos centros de estudio y se aleatorizaron para recibir Sterofundin® con glucosa al 1% o SS 0,9% con glucosa al 1%, de forma abierta. El resultado principal de la investigación fue determinar la variación electrolítica, principalmente la de cloro, que fue mayor con SS 0,9% (mediana 4; IQR 2, 6) en comparación con el grupo de Sterofundin® (mediana 2; IQR 1, 4) (p = 0,0001). En este caso concluyeron que Sterofundin® y SS 0,9% se pueden administrar con seguridad para el manejo intraoperatorio de fluidos en bebés y niños pequeños, pero la primera mostró un mejor perfil en la protección contra la acidosis metabólica, hipercloremia e hipomagnesemia36.
Sepsis y shock séptico
La mayoría de los niños ingresados con sepsis reciben reanimación inicial en un departamento de emergencias, donde el shock séptico sigue siendo una de las entidades más críticas tratadas por los médicos. La sepsis también es la afección hospitalaria más costosa y la causa más común del síndrome de disfunción orgánica múltiple (MODS, por sus siglas en inglés) pediátrico. Si bien todos los líquidos cristaloides ayudan a revertir el shock, se desconoce cuál es el tipo de reanimación con líquidos cristaloides más efectivo y seguro.
Trepatchayakorn et al.39 concluyeron en un estudio con 42 niños con shock séptico que, en la reanimación hídrica, la terapia en bolo de líquidos con cualquier tipo de solución cristaloide no produjo resultados diferentes. Sin embargo, cuando se administró un volumen superior a 30 mL/kg, el uso de RL se asoció con una reducción significativa de la lipocalina asociada a gelatinasa de neutrófilos urinaria (uNGAL), uno de los biomarcadores proteicos más novedosos y promisorios para la detección temprana de la injuria renal aguda37. En un estudio analítico de cohortes con emparejamiento por puntuación de propensión de pacientes pediátricos con sepsis o shock séptico, Fernández-Sarmiento et al.40 concluyeron que el uso de soluciones no balanceadas se asoció con un aumento de la frecuencia de lesión renal aguda en comparación con los niños que recibieron soluciones balanceadas (20,3% versus 25,7%; p= 0,006; ORa, 0,75; IC95%, 0,65-0,87), sin encontrar diferencias significativas en mortalidad, hipercloremia y acidosis metabólica40. En otro estudio donde se incluyeron 708 pacientes menores de 17 años con shock séptico bajo resucitación aleatorizada con fluidos, PlasmaLyte versus SS 0,9%, se demostró una reducción significativa en el riesgo de injuria renal aguda (20% versus 33%; RR 0,62; IC95% 0,48-0,80; p=0,0001) y requerimiento de terapia de reemplazo renal (10% versus 20%; RR 0,50; IC95% 0,34 a 0,73; p=0,0002) en el grupo de Plasmalyte. Sin embargo, la mortalidad en ambos grupos fue similar (33% versus 34%; RR 0,96; IC95% 0,78-1,19). Estos autores sugirieron escoger los cristaloides balanceados para la reanimación inicial con fluidos en shock séptico pediátrico11.
En otro estudio de cohorte retrospectivo con emparejamiento de datos, se investigaron 12.529 pacientes menores de 18 años con sepsis grave o shock séptico en 382 hospitales de Estados Unidos utilizando SS 0,9% versus RL. Después del emparejamiento, la mortalidad no fue diferente entre los grupos (7,2% versus 7,9%, cociente de riesgo 0,99; IC95% 0,98-1,01; p = 0,20). Se concluyó que la reanimación con RL no se asoció con mejores resultados en comparación con SS 0,9% en la sepsis pediátrica y se sugirió la conducción de ensayos prospectivos para su evaluación futura41. Emrath et al.6 concluyeron, en un análisis retrospectivo con 36.908 pacientes, realizado por emparejamiento de propensión, que el uso exclusivo de líquidos balanceados en pacientes pediátricos con sepsis durante las primeras 72 horas de reanimación se asoció con una mejor supervivencia, una menor prevalencia de lesión renal aguda y una duración más corta de las infusiones vasoactivas, en comparación con el uso exclusivo de SS 0,9%.
A pesar de la variada evidencia con el uso indistinto de fluidos cristaloides para la resucitación pediátrica en sepsis y shock séptico, y resultados opuestos en los dos estudios más grandes6,41, pareciera que el Pragmatic Pediatric Trial of Balanced versus Normal Saline Fluid in Sepsis (PRoMPT BOLUS)42 sería uno de los estudios futuros que podría inclinar la balanza. Se trata de un ensayo internacional de intervención, de etiqueta abierta, que se lleva a cabo en más de 40 sitios en los EE. UU., Canadá, Australia y Nueva Zelanda, y continuará durante 5 años. Incluirá a niños de 6 meses a 18 años aleatorizados para recibir cristaloides balaceados o SS 0,9%, tratados por sospecha de shock séptico con perfusión anormal. El resultado primario serán eventos renales adversos mayores dentro de los 30 días, mortalidad, terapia de reemplazo renal y disfunción renal persistente. Con una previsión de 8.800 pacientes, se convertirá en el estudio más grande hasta la fecha y, quizás, el que pueda brindar un poco más de luz al asunto del debate de las soluciones de reanimación en el shock séptico pediátrico42. Habrá que esperar entonces hasta el 2025 para realizar conclusiones sólidas; por ahora las soluciones balanceadas en la sepsis y shock séptico en pediatría solo han demostrado tener un discreto efecto protector en el desarrollo de la injuria renal aguda.
Resucitación con fluidos
La reanimación con líquidos es un componente fundamental del tratamiento de los pacientes en estado crítico, pero sigue siendo controvertido si la elección de los cristaloides afecta los resultados de los pacientes.
Una revisión exhaustiva reciente de Campos-Miño y Moreno43 sobre fluidos y electrólitos parenterales en pediatría con una visión abarcadora de la fisiología aplicada a la terapéutica sostiene que las recomendaciones actuales siguen apuntando a los fluidos balanceados como la estrategia de resucitación y mantenimiento principal para evitar situaciones como la acidosis metabólica hiperclorémica, así como afirman que estas soluciones contienen cierta cantidad de calcio que ayuda a tratar la hipocalcemia, los trastornos de la coagulación y la disfunción miocárdica43.
En 9 ensayos controlados aleatorizados analizados en el metanálisis de Liu et al.44, no hubo diferencias significativas en la mortalidad (riesgo relativo (RR) = 0,93, IC95% 0,86-1,01, p = 0,08), incidencia de insuficiencia renal aguda (RR 0,94; IC95% 0,88-1,00, p = 0,06), o la tasa de uso de TRR (RR 0,94, IC95% 0,69-1,27, p = 0,67) entre los grupos que utilizaron cristaloides balanceados y SS 0,9%. Entre 11.052 pacientes que fueron aleatorizados en 75 UCI de Brasil en un ensayo clínico aleatorizado, factorial, doble ciego, asignados 1:1, el uso de una solución balanceada en comparación con SS 0,9%, no redujo significativamente la mortalidad a los 90 días7. Lehr et al.45, en un metanálisis de tres ensayos controlados aleatorios con una población de 162 pacientes, encontraron un cambio mayor en el nivel de bicarbonato sérico (estimación combinada 1,60 mmol/L; IC95%, 0,04-3,16; p = 0,04) y en el pH (diferencia de medias combinada 0,03; IC95%, 0,00-0,06; p = 0,03) después de 4 a 12 horas de rehidratación con líquidos balanceados versus no balanceados. No encontraron diferencias en el nivel sérico de cloruro, lesión renal aguda, terapia de reemplazo renal o mortalidad.
Cloremia y mortalidad
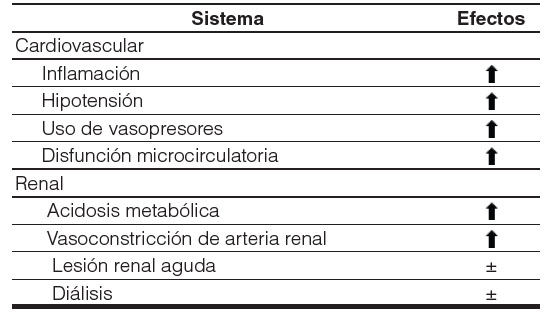
El cloruro tiene un papel importante en los mecanismos de retroalimentación glomérulo-tubular. A medida que aumenta la concentración de cloruro en el líquido del túbulo distal, se produce una retroalimentación a través de la mácula densa, la arteriola aferente se contrae y la tasa de filtración glomerular disminuye. Sin embargo, aún se desconoce si este evento adverso afecta la mortalidad y la incidencia de lesión renal aguda46. En un análisis retrospectivo de 890 niños con shock séptico en 29 unidades de cuidados intensivos pediátricos en los EE. UU., una media de cloruro mayor o igual a 110 mmol/L se asoció con mayores probabilidades de mortalidad (OR 2,1; IC95%, 1,3-3,5; p = 0,002)47.
Resultados similares encontraron Barhight et al48 en un estudio de cohorte retrospectivo de un solo centro en 66 niños en cuidados intensivos pediátricos que necesitaron terapia de reemplazo renal. La mortalidad fue significativamente mayor en los pacientes con hipercloremia (67%) en comparación con los que no la tenían (29%), p = 0,00648.
A pesar de la asociación de fluidos intravenosos ricos en cloruro e hipercloremia con aumento de la mortalidad, la hipocloremia también se asocia con resultados adversos. Los niveles bajos de cloruro sérico fueron un fuerte predictor de mortalidad en un estudio de seguimiento de 10 años de más de 9.000 adultos49. La fisiología subyacente a esta asociación queda por dilucidar, pero el efecto parece ser independiente de las concentraciones plasmáticas de sodio o potasio50,51.
La evidencia de las investigaciones retrospectivas citadas, recae en la asociación de mortalidad con niveles elevados o disminuidos de cloro, pero no pueden relacionar directamente la administración de SS 0,9% con la hipercloremia. Es necesario realizar más estudios prospectivos randomizados que persigan este objetivo.
CONCLUSIONES
Elegir el cristaloide adecuado para la fluidoterapia de resucitación en pediatría, puede marcar la diferencia en minimizar complicaciones ulteriores en el paciente. A diferencia de recientes resultados en estudios de adultos, la evidencia en niños ha demostrado que las soluciones balanceadas disminuyen el riesgo de lesión renal aguda y la necesidad de terapia de reemplazo renal. Existen sólidos resultados que respaldan el uso de soluciones balanceadas en la resucitación de la cetoacidosis diabética pediátrica. Las investigaciones sustentan además que no existen diferencias significativas sobre la mortalidad con el uso de ambos tipos de soluciones. A la espera de nuevos resultados de grandes ensayos clínicos aleatorizados en población pediátrica, se propone utilizar la fluidoterapia de resucitación con cristaloides en pediatría de manera individualizada, en respuesta al sustrato fisiológico de la entidad clínica de cada paciente.
Conflictos de interés
Los autores reportaron no tener ningún conflicto de interés, personal, financiero, intelectual, económico o corporativo en la realización de esta investigación.
Contribución de los autores
ACR: concepción y diseño del trabajo; recolección y obtención de resultados; análisis e interpretación de datos; redacción del manuscrito.
SCM: concepción y diseño del trabajo; revisión y redacción del manuscrito.
Financiamiento
Por los autores.