
ARTÍCULOS DE REVISIÓN
Revisión y cambios 2022 de las últimas
Guías de Resucitación Cardiopulmonar de la American Heart Association (AHA)
2022 Update of the Cardiopulmonary Resuscitation Guidelines by the American Heart Association (AHA)

ARTÍCULOS DE REVISIÓN
Guías de Resucitación Cardiopulmonar de la American Heart Association (AHA)
2022 Update of the Cardiopulmonary Resuscitation Guidelines by the American Heart Association (AHA)
Recibido: 06-12-2022
Aceptado: 12-12-2022
Publicado: 30-12-2022
Revista MetroCiencia
Volumen 30, Número 4, 2022
ISSNp: 1390-2989 ISSNe: 2737-6303
Editorial Hospital Metropolitano
Diego Villarreal Huato 1,
Mauricio Larrea2,
Santiago Campos-Miño3
RESUMEN
American Heart Association (AHA, por sus siglas en inglés) emite cada 5 años sus recomendaciones para resucitación cardiopulmonar (RCP) y atención cardiovascular de emergencia; la última versión se publicó en 20201. Sin embargo, cada cierto tiempo, un comité internacional (International Liaison Committee on Resuscitation – ILCOR) actualiza la bibliografía y emite ciertas recomendaciones de ajuste que son consideradas importantes. Estos cambios se han publicado el 4 de noviembre de este año en la revista Circulation2 y los resumimos a continuación, tanto para adultos como para niños.
Palabras clave: Resucitación cardiopulmonar; paro cardiaco; soporte vital básico; soporte vital pediátrico.
ABSTRACT
American Heart Association (AHA) publishes every five years its cardiopulmonary resuscitation and emergency cardiovascular care guidelines. The last version was published in 20201. However, the International Liaison Committee on Resuscitation (ILCOR) present a regular review of these guidelines and published several new recommendations and adjustments, being the last document published on November 4th, 20222, which is summarized here both for adults and children.
Keywords: Cardiopulmonary resuscitation; cardiac arrest; basic life support; pediatric life support.
Diego Villarreal Huato
 https://orcid.org/0000-0002-7137-3790
https://orcid.org/0000-0002-7137-3790
Mauricio Larrea
 https://orcid.org/0000-0003-2154-3621
https://orcid.org/0000-0003-2154-3621
Santiago Campos-Miño
 https://orcid.org/0000-0003-4686-7358
https://orcid.org/0000-0003-4686-7358
 |
Usted es libre de:Compartir — copiar y redistribuir el material en cualquier medio o formato. |
*Correspondencia: djvhmjat@gmail.com
ADULTOS
NIÑOS
Soporte vital básico
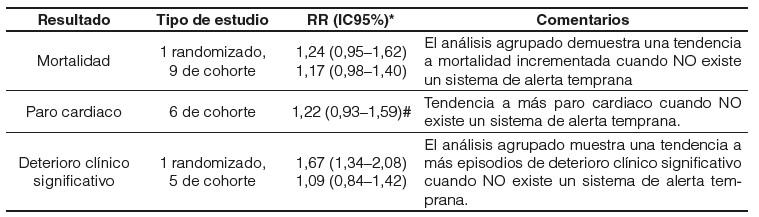
Tabla 1. Estudios que comparan la presencia versus la ausencia de sistemas de alerta temprana en pediatría y sus resultados.
Los siguientes puntos del algoritmo han sido revisados y aclarados.
Sugerimos no ordeñar el cordón umbilical antes de su pinzamiento para los bebés nacidos con menos de 28 semanas de edad gestacional.
No se recomienda la aspiración rutinaria oro/nasofaríngea para recién nacidos con secreciones claras o teñidas de meconio. La recomendación para la intubación y aspiración de meconio está dada solo en los casos que haya obstrucción de la vía aérea.
La mascarilla laríngea es una vía área alternativa efectiva cuando los intentos de ventilación con mascarilla facial o intubación no tienen éxito.